2020年05月08日讯 /生物谷BIOON/ --目前,新冠肺炎疫情仍在全球迅速蔓延。根据百度《新型冠状病毒肺炎疫情实时大数据报告》,截止2020年05月08日11时,全球累计确诊超过391万例,国外累计确诊超过383万例、死亡超过26.6万例。美国累计确诊129万例,死亡7.6万例。
全世界都在急切等待特效药的出现,其中对吉利德科学(Gilead Sciences)的抗病毒药物——“人民的希望”瑞德西韦(remdesvir)的呼声最高。该药的任何蛛丝马迹,都时刻牵动着大众紧绷的神经。
4月29日晚间,2项III期临床试验数据显示,瑞德西韦在治疗COVID-19患者方面具有疗效。根据该结果,美国FDA在5月初发布一份紧急使用授权(EUA),将瑞德西韦用于重症COVID-19住院患者的救治。吉利德已承诺免费捐赠总计150万剂瑞德西韦,这些药物目前正由美国政府调度和分发,以最大限度地为全美各大医院急需紧急治疗的患者提供治疗。
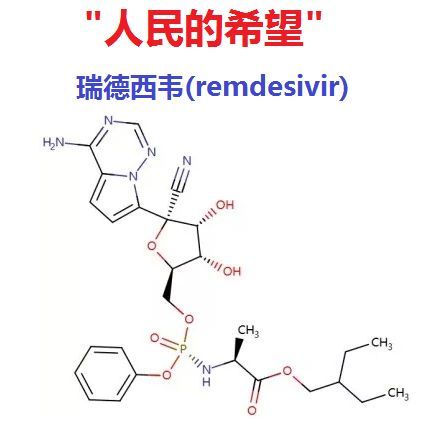
而在上述2项III期临床数据公布的几天前,日本首相安倍晋三已经喊话吉利德:只要提交申请,马上批准瑞德西韦!不曾想,幸福来得这么快!
5月7日,吉利德宣布,日本厚生劳动省(MHLW)已通过特殊审批途径,批准Veklury(remdesivir,瑞德西韦),作为新型冠状病毒(SARS-CoV-2)感染的治疗药物,SARS-CoV-2是导致新型冠状病毒肺炎的病毒。特殊批准的授予归因于新型冠状病毒肺炎的大流行,其参考了瑞德西韦在美国的紧急使用授权(EUA)。
此次批准,基于:(1)美国国家过敏和传染病研究所(NIAID)开展的一项治疗COVID-19中重度症状患者(包括危重患者)的安慰剂对照全球III期临床试验数据;(2)吉利德开展的一项治疗重症COVID-19患者的开放标签全球III期试验数据;(3)吉利德同情用药项目(包括日本患者)的现有数据。
吉利德科学首席医疗官Merdad Parsey医学博士表示:“日本批准瑞德西韦(remdesivir)是基于在日本治疗危重患者的迫切需要。这反映了此次疾病大流行的特殊情况。我们感谢日本厚生劳动省,在与我们共同应对这一公共卫生紧急事件中的领导力与合作精神。”
由于目前的公共卫生紧急状况,美国食品和药物管理局(FDA)已对瑞德西韦进行紧急使用授权(EUA)用于治疗新型冠状病毒肺炎。在美国,瑞德西韦是一种在研药物,尚未获得FDA批准用于任何用途,其用于治疗新型冠状病毒肺炎的安全性和有效性尚未确定。在美国,瑞德西韦仅获得授权用于治疗新型冠状病毒肺炎重症的住院患者。关于瑞德西韦在美国授权使用的其他重要信息请参见下文。
瑞德西韦在日本以外的国家尚未获得许可或批准,正在进行的临床试验仍在继续评估其安全性和有效性。吉利德持续与全球监管机构合作,以确保恰当的瑞德西韦的可及性。
关于瑞德西韦:
瑞德西韦是一种在研的核苷酸类似物,具有广谱抗病毒活性,其在体外和动物模型的体内研究中显示了对多种新出现的病毒病原体的效果,包括埃博拉病毒、马尔堡病毒、中东呼吸综合征(MERS)和非典型性肺炎(SARS)病毒。吉利德进行的体外试验表明,瑞德西韦对 SARS-CoV-2具有活性。多个正在进行中的三期临床试验正在评估瑞德西韦治疗新型冠状病毒肺炎的安全性和有效性。
关于瑞德西韦在美国的重要信息
瑞德西韦(GS-5734™)获得了一项紧急使用授权,用于治疗疑似或者实验室确诊的SARS-CoV-2感染和重症新型冠状病毒肺炎。SARS-CoV-2是导致新型冠状病毒肺炎疾病的冠状病毒。重症的定义为患者在室内空气条件下的氧气饱和度(SpO2)≤ 94%、或需要氧气支持、或需要机械通气、或需要接受体外肺膜氧合(ECMO)。瑞德西韦必须通过静脉注射,其被批准用于已收治入院且可以接受临床静脉注射的成人或儿童患者。
瑞德西韦是一种在研药物,尚未被FDA批准。关于瑞德西韦治疗新型冠状病毒肺炎的安全性和有效性尚未明确。瑞德西韦仅被授权用于证明紧急使用授权成立的情况声明期间,除非该授权被中止或者更早地撤销。
关键词:吉利德 瑞德西韦
分享至:
![]()
![]()




鄂公网安备 42011102004299号
© 2014-2025 前衍化学科技(武汉)有限公司 版权所有 鄂ICP备20009754号-1